A Caixa começou a pagar neste domingo, dia 17, a parcela de setembro do Auxílio Brasil. Recebem hoje os beneficiários com Número de Inscrição Social (NIS) com final 1. Esta é a segunda parcela com o valor mínimo de R$ 600, que vai vigorar até dezembro deste ano, conforme emenda constitucional promulgada em julho.
No cronograma, a data de pagamento seria na segunda-feira (19). No entanto, segundo a Agencia Brasil, a Caixa informou que as parcelas com data de validade com início nas segundas-feiras ficam disponíveis para movimentação a partir do sábado imediatamente anterior. De acordo com o banco, essa situação é permanente e foi apresentada “anteriormente ao início do programa, não se tratando de excepcionalidade para o mês corrente”.
O beneficiário poderá consultar informações sobre as datas de pagamento, o valor do benefício e a composição das parcelas em dois aplicativos: Auxílio Brasil, desenvolvido para o programa social, e o aplicativo Caixa Tem, usado para acompanhar as contas poupança digitais do banco.
Metro1







 Foto: Leonardo Sá/ Agência Senado
Foto: Leonardo Sá/ Agência Senado  Foto: Ricardo Stuckert
Foto: Ricardo Stuckert  Imagem ilustrativa de Wokandapix por Pixabay
Imagem ilustrativa de Wokandapix por Pixabay 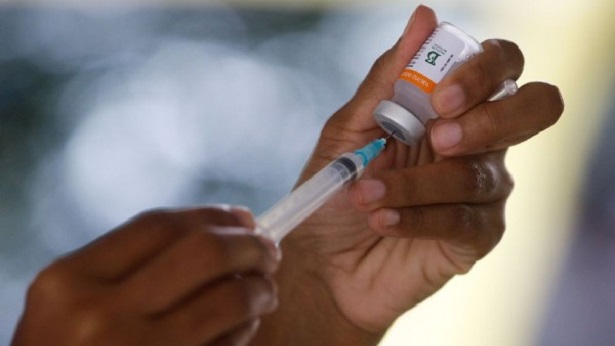 Foto: Tânia Rego/ Agência Brasil
Foto: Tânia Rego/ Agência Brasil  Foto: Marcelo Camargo/ Agência Brasil
Foto: Marcelo Camargo/ Agência Brasil  Foto: Marcello Casal Jr/ Agência Brasil
Foto: Marcello Casal Jr/ Agência Brasil